Đình chỉ lưu hành, thu hồi nhiều thuốc, mỹ phẩm
- Pháp luật
 19:45 - 07/05/2020
19:45 - 07/05/2020

ảnh minh họa.
Cụ thể, dung dịch kháng khuẩn All Clean (số lô 84202, ngày sản xuất 24/3/2020, hạn dùng 36 tháng kể từ ngày sản xuất) do Công ty TNHH Dược mỹ phẩm Nam Khang sản xuất và chịu trách nhiệm đưa sản phẩm ra thị trường bị đình chỉ lưu hành và thu hồi trên toàn quốc do kết quả kiểm nghiệm mẫu thử không đáp ứng yêu cầu về hàm lượng methanol 41%.
Cục Quản lý dược yêu cầu Công ty Nam Khang phải khẩn trương gửi thông báo thu hồi tới những nơi phân phối, sử dụng sản phẩm nói trên và gửi báo cáo thu hồi sản phẩm trên về Cục trước ngày 31/5.
Sản phẩm thứ hai bị thu hồi toàn quốc là thuốc Dekasiam (Acid acetylsalicylic 100mg, số đăng ký VD-22510-15, số lô 101218, hạn dùng 13/12/2020) do Công ty cổ phần Dược phẩm Sao Kim sản xuất. Mẫu thuốc không đạt tiêu chuẩn chất lượng về chỉ tiêu độ hòa tan, tạp chất liên quan, định lượng (vi phạm mức độ 2).
Dekasiam là thuốc được sử dụng dự phòng nhồi máu cơ tim thứ phát và đột quỵ trong các trường hợp có tiền sử bị nhồi máu cơ tim (đau tim), có tiền sử bị đột quỵ do thiếu máu não cục bộ hoặc đột quỵ do thiếu máu não thoáng qua (đột quỵ nhẹ), đau thắt ngực ổn định hoặc không ổn định, đã phẫu thuật tim như thủ thuật tạo hình mạch hay phẫu thuật đặt ống tim.
Cục Quản lý dược yêu cầu Công ty Sao Kim phối hợp với nhà phân phối thuốc gửi thông báo thu hồi tới các cơ sở bán buôn, bán lẻ, sử dụng lô thuốc nói trên và thu hồi toàn bộ lô thuốc không đạt tiêu chuẩn chất lượng này và gửi báo cáo thu hồi về Cục trước ngày 27/5.
Lô sản phẩm Kem mụn thâm Linh Nga hộp 12g (số lô 01, ngày sản xuất 2/1/2018, hạn sử dụng 2/1/2021) do Cơ sở hóa mỹ phẩm Linh Nga sản xuất và chịu trách nhiệm đưa sản phẩm ra thị trường cũng bị Cục Quản lý dược ra thông báo đình chỉ lưu hành do mẫu thử không đáp ứng quy định về chỉ tiêu khối lượng trung bình và độ đồng đều khối lượng.
Cục Quản lý dược yêu cầu Cơ sở hóa mỹ phẩm Linh Nga phải gửi thông báo thu hồi tới những nơi phân phối, sử dụng sản phẩm nêu trên và thu hồi toàn bộ lô sản phẩm mỹ phẩm không đáp ứng quy định và gửi báo cáo thu hồi về Cục trước ngày 31/5.
Ngoài yêu cầu các cơ sở thu hồi sản phẩm không đạt chất lượng, Cục Quản lý dược cũng đề nghị sở y tế các tỉnh, thành phố thông báo cho các cơ sở kinh doanh, sử dụng các sản phẩm nói trên thu hồi lô sản phẩm không đạt chất lượng; kiểm tra, giám sát các đơn vị thực hiện thông báo này; xử lý các đơn vị vi phạm theo quy định hiện hành.
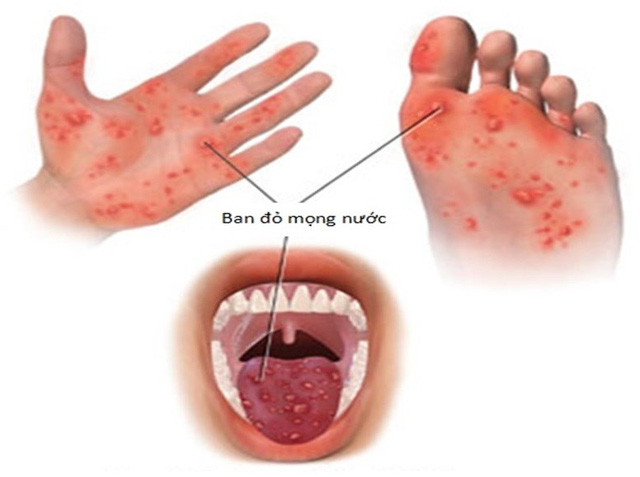
Cảnh báo bệnh tay chân miệng bùng phát mùa hè: cha mẹ cần biết gì?
 1 năm trước
1 năm trước